JAK chinasi per la vitiligine
Nuove prospettive
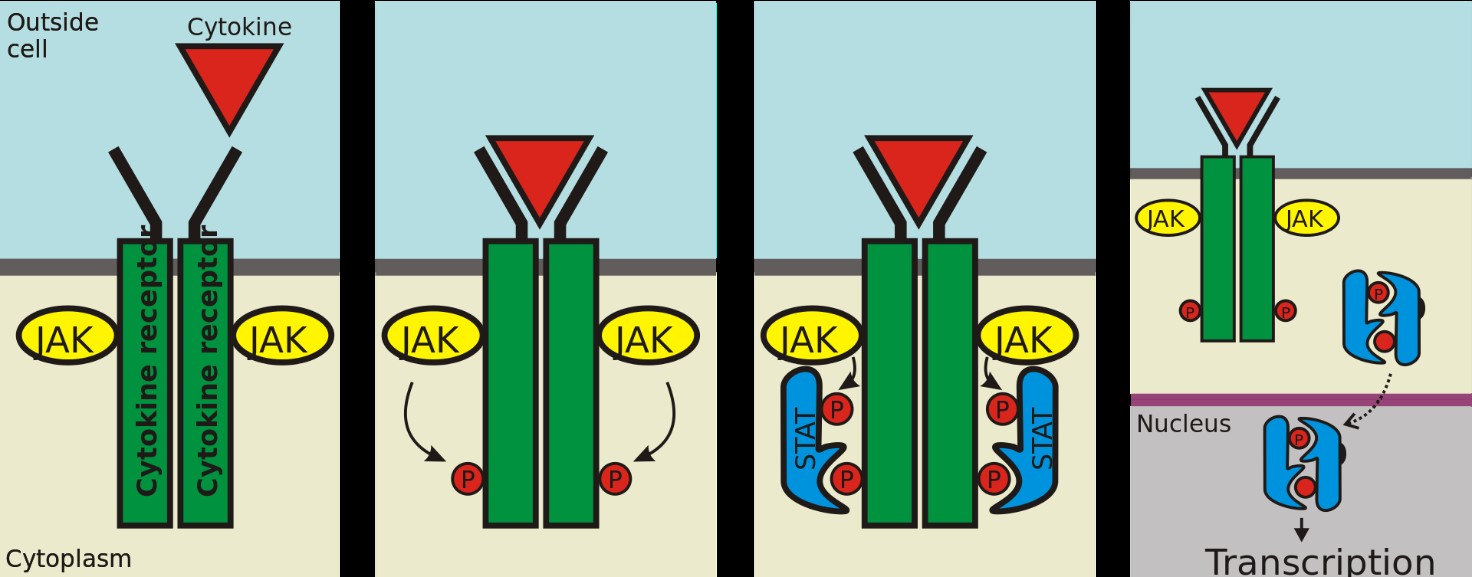
Gli inibitori delle "just another kinase", Janus chinasi, (JAK) sono una classe di farmaci che agiscono inibendo l'attività di uno o più componenti di una famiglia di enzimi, le tirosin-chinasi non recettoriali che trasducono i segnali mediati dalle citochine attraverso la via metabolica JAK-STAT. Attraverso questa via le citochine pro-infiammatorie (TNF-α, IL-1, IL-6 e IFN-γ) espletano la loro azione.
I JAK inibitori o anti JAK a differenza dei farmaci biologici (costituiti da proteine che impediscono l’infiammazione bloccando i recettori situati all’esterno della cellula) interagiscono con specifici recettori enzimatici all’interno della cellula, bloccando una serie di reazioni chimiche responsabili dell’attivazione della risposta infiammatoria.
Gli inibitori delle JAK chinasi vengono utilizzati in oncologia e nel trattamento di alcune patologie infiammatorie quali psoriasi, artrite psoriasica, dermatite atopica, artrite reumatoide, spondiloartriti, artrite idiopatica giovanile, spondilite anchilosante, spondiloartrite assiale non radiografica, colite ulcerosa, dermatite atopica, alopecia areata, artriti in corso di malattie infiammatorie croniche intestinali, disturbi mieloproliferativi.
Questi farmaci hanno un profilo di sicurezza simile a quello dei farmaci biologici. Sembrano essere ben tollerati anche se, in alcuni casi durante la terapia con Jak Inibitore è stato osservato un aumento del rischio di tromboembolia.
Come per i farmaci biologici, sono previsti screening infettivologici anche nei pazienti in terapia con JAK inibitore. Gli screening sono gli stessi utilizzati per la maggior parte dei farmaci biologici ed in particolare è raccomandato lo screening per la tubercolosi latente. Circa il rischio di herpes zoster, nei pazienti con evidenziato rischio di questo tipo di infezione è indicata la vaccinazione prima di iniziare la terapia. Prima e durante le prime fasi della terapia è anche consigliato il controllo del colesterolo il cui valore potrebbe aumentare in corso di terapia. Solitamente l’aumento dei valori è reversibile.
Durante la gravidanza o durante l’allattamento i JAK inibitori sono sconsigliati, pertanto è indicata la contraccezione e la programmazione della eventuale gravidanza una volta terminata la terapia.
Diversi studi e segnalazioni hanno evidenziato un’aumentata incidenza di neoplasie maligne, eventi avversi cardiovascolari maggiori (MACE), infezioni gravi, tromboembolismo venoso (TEV) e mortalità in pazienti con artrite reumatoide (AR) e sono sottoposti a trattamento con JAK inibitori rispetto a coloro che assumono inibitori del TNF-alfa.
Alla luce di queste evidenze, l’Agenzia italiana del farmaco (Aifa) ha pubblicato una importante nota informativa: i JAK inibitori devono essere utilizzati solo nel caso in cui non siano disponibili alternative terapeutiche appropriate ed in particolar modo in pazienti di età pari o superiore a 65 anni; fumatori o che sono stati fumatori per molto tempo; soggetti con altri fattori di rischio cardiovascolare o di neoplasia maligna. I medici prescrittori devono informare i pazienti dei rischi associati all’uso di JAK inibitori. A tutti i pazienti si raccomanda un esame dermatologico periodico.
Farmaci approvati
Ruxolitinib contro JAK1/JAK2 mielofibrosi, e artrite reumatoide. Approvato dalla FDA degli Stati Uniti nel novembre 2011 per mielofibrosi (intermedia o ad alto rischio) e policitemia vera, in pazienti con risposta inadeguata o intolleranti all'idrossiurea.
Tofacitinib (precedentemente noto come CP-690550) contro JAK3 per la psoriasi e l'artrite reumatoide. La FDA statunitense lo ha approvato nel novembre 2012 per l'artrite reumatoide (da moderatamente a gravemente attiva) in pazienti che avevano una risposta inadeguata o intolleranza al metotrexato.
Oclacitinib - contro JAK1 per il controllo del prurito associato a dermatite allergica e il controllo della dermatite atopica nei cani di almeno 12 mesi di età.
Baricitinib contro JAK1 e JAK2 per l'artrite reumatoide.
Peficitinib (ASP015K, JNJ-54781532) inibisce principalmente JAK3 e viene usato per il trattamento dell'artrite reumatoide. Approvato per l'uso in Giappone nel 2019.
Fedratinib (SAR302503) è un inibitore JAK2 per il trattamento della mielofibrosi primaria (incluso in pazienti precedentemente trattati con ruxolitinib) o mielofibrosi secondaria (post-policitemia vera o trombocitemia post-essenziale). Approvata dalla US FDA il 16 agosto 2019.
Upadacitinib (ABT-494) contro JAK1 per l'artrite reumatoide. Approvato dalla FDA degli Stati Uniti il 16 agosto 2019.
Abrocitinib (PF-04965842) contro JAK1 per dermatite atopica e psoriasi da moderata a grave. Approvato dall'FDA nel 2022.
Farmaci in sperimentazione
Filgotinib (G-146034, GLPG-0634) contro JAK1 per l'artrite reumatoide e la malattia di Crohn.
Cerdulatinib (PRT062070) doppio inibitore SYK e JAK per neoplasie ematologiche.
Gandotinib (LY-2784544) contro JAK2 per neoplasie mieloproliferative.
Lestaurtinib (CEP-701) contro JAK2 per leucemia mieloide acuta (LMA).
Momelotinib (GS-0387, CYT-387) contro JAK1 e JAK2 per disturbi mieloproliferativi e carcinoma pancreatico metastatico recidivante/refrattario.
Pacritinib (SB1518) contro JAK2 per linfoma recidivante e neoplasie mieloidi avanzate, anche mielofibrosi, neoplasie mieloproliferative e sindrome mielodisplastica.
Farmaci indicati in off label
Cucurbitacina I (JSI-124).
CHZ868 - inibitore JAK2 di tipo II per l'uso in disturbi mieloproliferativi e leucemia mielomonocitica cronica (CMML).
Tofacitinib per alopecia universalis.
Tofacitinib e ruxolitinib topici per l'alopecia.
Ruxolitinib topico per la vitiligine.
Si ritiene che l’iperattività della via di segnale JAK guidi l’infiammazione coinvolta nella patogenesi e nella progressione della vitiligine, malattia autoimmune cronica caratterizzata da depigmentazione cutanea e formazione di chiazze bianco latte per la progressiva distruzione dei melanociti.
Nell’Unione Europea si stima che la prevalenza della vitiligine diagnosticata sia di circa 1,5 milioni di pazienti di cui circa 8 su 10 soffrono di vitiligine non segmentale, e un sottogruppo di questi presenta un coinvolgimento del viso. La vitiligine può verificarsi a qualsiasi età, anche se molti pazienti con vitiligine manifestano i primi sintomi prima dei 30 anni.
Ruxolitinib crema è il primo trattamento approvato nell’Unione Europea per la ripigmentazione nella vitiligine non segmentale. La decisione della Commissione Europea si basa sui dati di due studi clinici registrativi di fase 3 – TRuE-V1 e TRuE-V2 – che hanno valutato l’efficacia e la sicurezza di ruxolitinib crema in più di 600 persone con vitiligine non segmentale, di età pari o superiore a 12 anni.
Il Ruxolitinib crema all'1,5% (15 mg/g) è una nuova formulazione topica dell'inibitore selettivo JAK1/JAK2. Approvato dalla Fda per il trattamento topico della vitiligine non segmentale in pazienti con almeno 12 anni di età è il primo e unico trattamento per la ripigmentazione cutanea. Negli Stati Uniti è anche autorizzato per il trattamento topico cronico a breve termine e non continuativo della dermatite atopica da lieve a moderata, in pazienti non immunocompromessi, dai 12 anni di età in poi, la cui malattia non è adeguatamente controllata con terapie topiche o quando queste non sono consigliabili. Non sono stati segnalati eventi avversi gravi correlati al trattamento con ruxolitinib crema. La reazione avversa più comune è stata acne nella sede di applicazione. Nell’alopecia areata, è stato osservato che il Ruxolitinib provoca la ricrescita dei capelli ma la sospensione del trattamento porta il ritorno dell’alopecia areata con la formazione delle chiazze prive di capelli.
Bibliografia
• Kontzias A, Kotlyar A, Laurence A, Changelian P, O'Shea JJ, Jakinibs: a new class of kinase inhibitors in cancer and autoimmune disease, in Current Opinion in Pharmacology, vol. 12, n. 4, agosto 2012, pp. 464-70, DOI:10.1016/j.coph.2012.06.008, PMC 3419278, PMID 22819198.
• Norman P, Selective JAK inhibitors in development for rheumatoid arthritis, in Expert Opinion on Investigational Drugs, vol. 23, n. 8, agosto 2014, pp. 106777, DOI:10.1517/13543784.2014.918604 PMID 24818516.
• Vaddi K, Sarlis NJ, Gupta V, Ruxolitinib, an oral JAK1 and JAK2 inhibitor, in myelofibrosis, in Expert Opinion on Pharmacotherapy, vol. 13, n. 16, novembre 2012, pp. 2397-407, DOI:10.1517/14656566.2012.732998, PMID 23051187.
• Zerbini CA, Lomonte AB, Tofacitinib for the treatment of rheumatoid arthritis, in Expert Review of Clinical Immunology, vol. 8, n. 4, maggio 2012, pp. 319-31, DOI:10.1586/eci.12.19, PMID 22607178.
• Gonzales AJ, Bowman JW, Fici GJ, Zhang M, Mann DW, Mitton-Fry M, Oclacitinib (APOQUEL(®)) is a novel Janus kinase inhibitor with activity against cytokines involved in allergy, in Journal of Veterinary Pharmacology and Therapeutics, vol. 37, n. 4, agosto 2014, pp. 317-24, DOI:10.1111/jvp.12101, PMC 4265276, PMID 24495176.
• FDA Approves Apoquel (oclacitinib tablet) to Control Itch and Inflammation in Allergic Dogs, su news.zoetis.com, Zoetis, 16 maggio 2013. URL consultato il 23 febbraio 2017 (archiviato dall'url originale il 23 febbraio 2017).
• FDA Approves OLUMIANT® (baricitinib) 2-mg Tablets for the Treatment of Adults with Moderately-to-Severely Active Rheumatoid Arthritis, su Eli Lilly and Company, 1º giugno 2018. URL consultato il 21 agosto 2018.
• Genovese MC, Greenwald M, Codding C, Zubrzycka-Sienkiewicz A, Kivitz AJ, Wang A, Shay K, Wang X, Garg JP, Cardiel MH, Peficitinib, a JAK Inhibitor, in Combination With Limited Conventional Synthetic Disease-Modifying Antirheumatic Drugs in the Treatment of Moderate-to-Severe Rheumatoid Arthritis, in Arthritis & Rheumatology, vol. 69, n. 5, maggio 2017, pp. 932-942, DOI:10.1002/art.40054, PMID 28118538.
• Markham A, Keam SJ, Peficitinib: First Global Approval, in Drugs, vol. 79, n. 8, giugno 2019, pp. 887-891, DOI:10.1007/s40265-019-01131-y, PMID 31093950.
• FDA approves treatment for patients with rare bone marrow disorder, su FDA, 16 agosto 2019. URL consultato il 16 agosto 2019.
• U.S. FDA Approves INREBIC® (Fedratinib) as First New Treatment in Nearly a Decade for Patients With Myelofibrosis, su ir.celgene.com. URL consultato il 16 agosto 2019 (archiviato dall'url originale il 16 agosto 2019).
• Harel S, Higgins CA, Cerise JE, Dai Z, Chen JC, Clynes R, Christiano AM, Pharmacologic inhibition of JAK-STAT signaling promotes hair growth, in Science Advances, vol. 1, n. 9, ottobre 2015, pp. e1500973, Bibcode:2015SciA....1E0973H, DOI:10.1126/sciadv.1500973, PMC 4646834, PMID 26601320.
• Shreberk-Hassidim R, Ramot Y, Zlotogorski A, Janus kinase inhibitors in dermatology: A systematic review, in Journal of the American Academy of Dermatology, vol. 76, n. 4, aprile 2017, pp. 745–753.e19, DOI:10.1016/j.jaad.2016.12.004, PMID 28169015.
• Liu M et al. Janus Kinase Inhibitors for Alopecia Areata: A Systematic Review and Meta-Analysis. JAMA Netw Open. 2023 Jun 1;6(6):e2320351.
Dott.ssa Flora De Natale - Specialista in Dermatologia e Venereologia - Vicepresidente ADECA
Dott. Mariano Saviano - Specialista in Dermatologia e Venereologia – Coordinatore Gruppo Adecanews ADECA