Emangiomi
Malattie rare: Emangiomi e sindromi
Introduzione
Gli emangiomi infantili (EI) sono i tumori vascolari benigni più comuni nei neonati e si distinguono per una peculiare storia naturale che li rende unici tra le anomalie vascolari. Sebbene la maggior parte degli EI sia innocua e autorisolutiva, alcune manifestazioni possono comportare complicanze significative o associarsi a sindromi rare e complesse, come PHACE e LUMBAR/PELVIS. Queste condizioni richiedono un’attenta valutazione multidisciplinare per una gestione adeguata.
Questo articolo, redatto dalla sezione malattie rare del gruppo dermatologico ADECA, analizza l’epidemiologia, la storia naturale, la diagnosi e il trattamento degli EI, con un focus particolare sulle sindromi associate, il ruolo dell'HIRES score per la stratificazione del rischio e le indicazioni alla terapia.
1.1 Definizione e caratteristiche generali
Emangioma deriva dal greco antico αίμα (sangue), ἀγγεῖον (vaso) e ὄγκοϛ (massa o tumore). Gli emangiomi infantili (EI) rientrano nel capitolo dei tumori vascolari: la classificazione adottata dalla “International Society for the Study of Vascular Anomalies” (ISSVA), e successivamente aggiornata ed ampliata nel 2018 suddivide tali tumori in benigni, localmente aggressivi e maligni. Gli emangiomi infantili sono i tumori vascolari più comuni, seguiti dagli emangiomi "congeniti", che comprendono l'emangioma congenito a rapida involuzione (RICH), l'emangioma congenito non involutivo (NICH) e l’emangioma congenito parzialmente involutivo (PICH). Gli emangiomi infantili congeniti sono clinicamente, geneticamente e istopatologicamente distinti dagli emangiomi infantili. Una delle principali differenze cliniche è rappresentata dal fatto che i primi sono completamente sviluppati alla nascita e spesso rilevabili con l'ecografia prenatale, mentre gli emangiomi infantili, si evidenziano alla nascita, con un "precursore”.Gli emangiomi infantili sono caratterizzati da una fase di crescita e una fase di involuzione, al contrario delle malformazioni vascolari, anomalie strutturali derivanti da capillari, arterie, vene, vasi linfatici che crescono in proporzione al bambino e non regrediscono.
1.2 Epidemiologia
Gli emangiomi sono i tumori più comuni dell'infanzia. La vera incidenza degli emangiomi infantili non è nota: si dice classicamente che interessano fino al 10 % dei bambini caucasici. Gli emangiomi infantili sono generalmente osservati entro i primi giorni o mesi di vita. Sebbene la maggior parte degli emangiomi si verifichi sporadicamente, è stata segnalata la trasmissione familiare con modalità autosomica dominante: in una serie di 136 famiglie, il 34% aveva una storia familiare di EI. Gli emangiomi sono da due a tre volte più comuni tra le femmine rispetto ai maschi e per ragioni sconosciute, nel sesso femminile, sono anche più probabili le complicanze. Gli emangiomi sono più comuni tra i bambini bianchi non ispanici rispetto ad altri gruppi razziali. L'incidenza di emangiomi risulta piu’ alta nei prematuri e nei nati da gravidanze gemellari. Altri fattori di rischio sono l’età materna avanzata, la placenta previa, la preeclampsia e altre anomalie placentari. La villocentesi così come le altre procedure invasive, non sembra svolgere un ruolo significativo nello sviluppo della maggior parte degli emangiomi. Due sindromi sono associate a un'aumentata frequenza di EI: la sindrome PHACES (posterior fossa malformations, hemangioma, arterial anomalies, coarctation of the aorta/cardiac defects, eye abnormalities and sternal maformations) e la sindrome LUMBAR (Lower body hemangioma, Urogenital abnormalities, Myelopathy, Bony deformities, Anorectal malformations and Rectal anomalies).
1.3 Patogenesi
Gli emangiomi sono caratterizzati da una fase di proliferazione ed una di involuzione. Molteplici evidenze suggeriscono che l'ipossia possa avere un ruolo chiave nella patogenesi degli emangiomi, inclusi dati epidemiologici riguardo l’associazione degli emangiomi infantili con condizioni correlate all'ipossia placentare (p. es., basso peso alla nascita, retinopatia del prematuro, gravidanze multiple, anomalie placentari) ed il riconoscimento immunoistochimico, sugli emangiomi proliferanti, di bersagli multipli del Fattore Inducibile dall'ipossia -1alfa, come il fattore di crescita endoteliale vascolare (VEGF)-A, l'isoforma 1 del trasportatore del glucosio (GLUT1) ed il fattore di crescita simile all'insulina-2 (IGF-2). È stato proposto che l'ipossia in utero o l'ipossia locale possano essere il fattore scatenante per lo sviluppo di emangiomi, con la fase proliferativa che è un tentativo omeostatico di normalizzare il tessuto ipossico. Il GLUT1 e gli antigeni vascolari associati alla placenta (recettore Fc-gamma II, merosina e antigene Lewis Y) sono altamente espressi nelle cellule endoteliali degli emangiomi infantili, sia durante la fase proliferativa che in quella involutiva. Questi marcatori non sono espressi nei normali capillari dermici o sottocutanei, né sono espressi in altri tipi di tumori vascolari. Le evidenze attuali suggeriscono che gli emangiomi sono proliferazioni clonali di cellule endoteliali, derivanti dalla vasculogenesi (la formazione di vasi sanguigni primitivi dagli angioblasti), piuttosto che dall'angiogenesi (la crescita di nuovi vasi da vasi preesistenti) come tradizionalmente pensato. Questa ipotesi è supportata da uno studio in cui l'impianto di cellule staminali multipotenziali da tessuto di emangioma umano (isolate in base all'espressione di CD133, un marker di popolazione di cellule staminali) ha dato origine a lesioni simil-emangioma in topi immunodeficienti che sono regrediti spontaneamente, in modo simile a quanto accade negli emangiomi infantili. La proliferazione dell'emangioma sembra derivare da uno squilibrio tra fattori vasculogenici positivi e negativi espressi dall'emangioma e dal tessuto normale adiacente.
1.4 Clinica
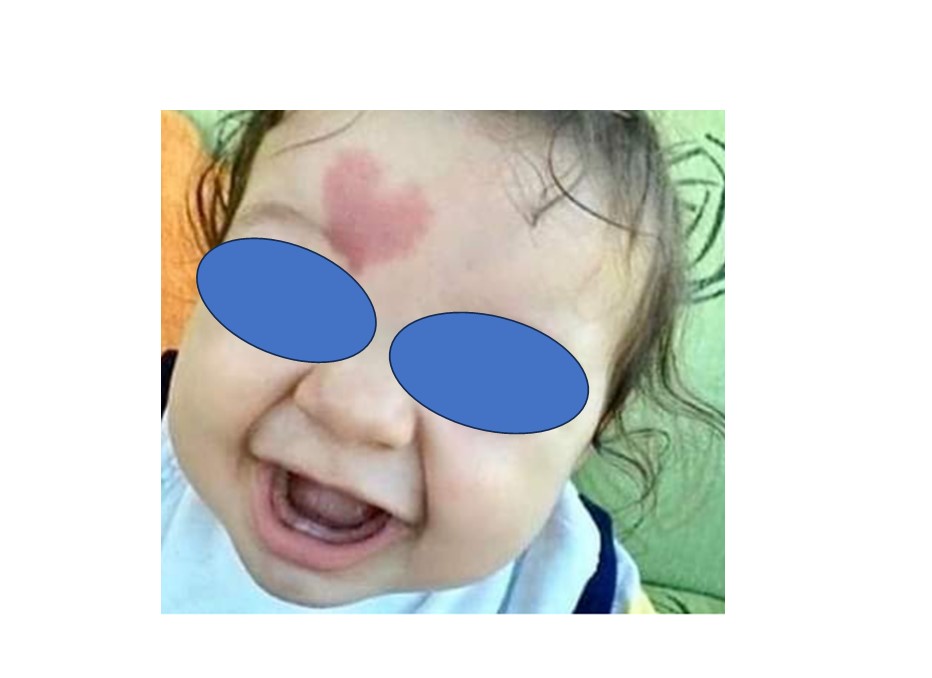
La maggior parte degli emangiomi non è clinicamente evidente alla nascita, ma si manifesta entro i primi giorni o mesi di vita. Alcuni neonati possono mostrare un precursore, ossia una chiazza anemica, roseo pallida o bluastra, che può essere ricoperta da teleangectasie e circondata da un alone di pallore circostante (secondario alla vasocostrizione). Le lesioni precoci possono essere così poco evidenti da non essere riconosciute o possono essere scambiate per un graffio o un livido. Meno comunemente, un emangioma può apparire inizialmente come una macula rossastra confondibile con una port wine stain o macchia vino porto. La maggior parte delle lesioni sono solitarie, ma lesioni multiple si verificano fino al 20% dei neonati. Gli emangiomi hanno una predilezione per la testa e il collo, sebbene possano verificarsi ovunque sulla cute, mucose e/o organi interni. Gli emangiomi variano in dimensioni da pochi millimetri a vari centimetri di diametro. Possono essere superficiali, profondi e misti. La presentazione superficiale è la più comune e consiste in una papula, un nodulo od una placca di colorito rosso o rosso-violaceo, a superficie liscia o lobulata, di consistenza teso elastica; raramente la base è peduncolata. Le dimensioni sono variabili, da pochi millimetri sino al coinvolgimento di un’area estesa (intero arto, emitronco, etc.). L'emangioma profondo, o sottocutaneo, è tipicamente un nodulo rilevato, coperto da cute di colorito normale, che spesso mostra una sfumatura di tonalità bluastra con o senza teleangectasie. Gli emangiomi puramente profondi sono meno comuni. Gli emangiomi misti sono abbastanza comuni e mostrano una doppia componente, sia superficiale che profonda. Gli emangiomi possono inoltre essere classificati inoltre in base all’estensione, come localizzati (o focali), segmentali o multipli. Gli emangiomi localizzati, che costituiscono la maggior parte dei casi, mostrano un’estensione circoscritta e ben definita e sembrano derivare da un singolo focus. Gli emangiomi segmentali si presentano come chiazze o placche che vanno a coinvolgere uno specifico distretto cutaneo. Sono stati identificati quattro distinti modelli segmentali per quanto riguarda il distretto cranio-faciale:
- Segmento 1, che coinvolge la fronte laterale, il cuoio capelluto temporale anteriore e il cuoio capelluto frontale-laterale;
- Segmenti 2 e 3, corrispondenti al mascellare e mandibolare;
- Segmento 4, che coinvolge il cuoio capelluto frontale mediale, il naso ed il filtro.
Gli emangiomi segmentali hanno maggiori probabilità di colpire il sesso femminile e, rispetto alle lesioni localizzate, è molto più probabile che siano associati a complicanze. I bambini con emangiomi segmentali richiedono generalmente una terapia più impegnativa e protratta, mostrando un outcome peggiore rispetto ai bambini con emangiomi focali. Posso inoltre rientrare a far parte di quadri malformativi più complessi, associandosi ad anomalie di altri organi (cuore, cervello), come la Sindrome PHACES definita dalla presenza di un grande, emangioma segmentale, di solito del volto, in associazione con una o più malformazioni congenite, più comunemente malformazioni strutturali o cerebrovascolari del cervello. Il segno distintivo della sindrome PHACES, un ampio emangioma segmentale del viso, può coinvolgere da uno a più dermatomi facciali.
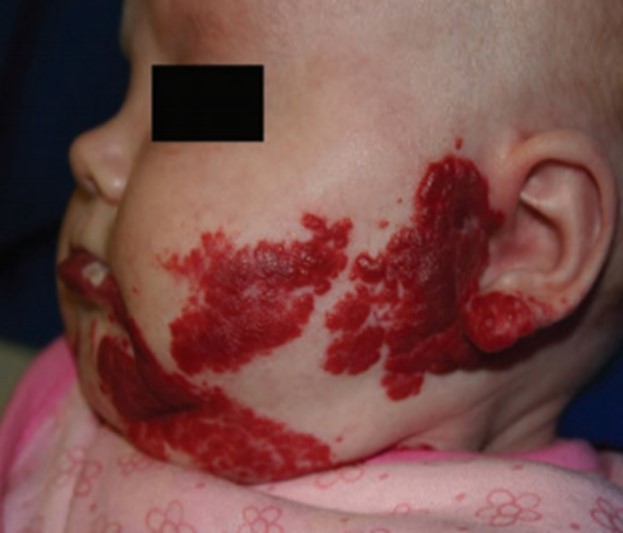
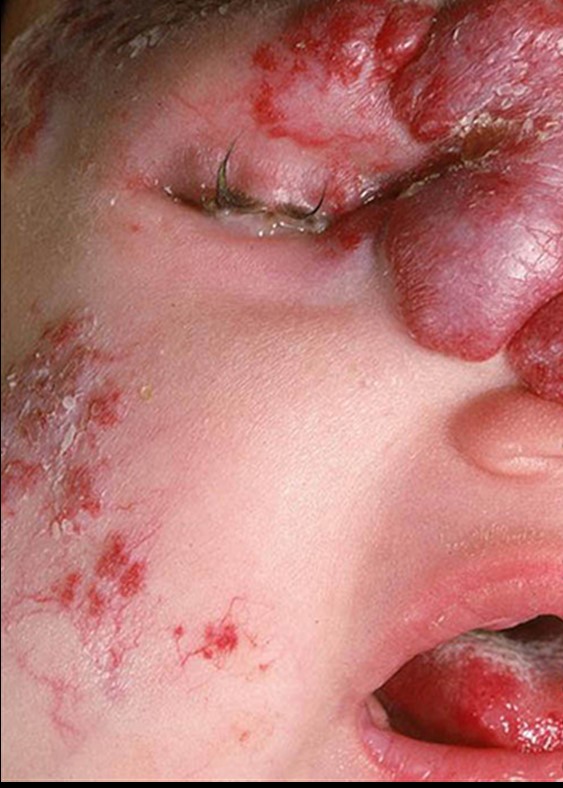
Gli emangiomi che si sviluppano lungo la linea mediana della colonna vertebrale rappresentano l’elemento caratterizzante di altre condizioni multisistemiche quali la PELVIS (perineal hemangioma, external genitalia malformations, lipomyelomeningocele, vesicorenal abnormalities, imperforate anus, and skin tag), la SACRAL (spinal dysraphism, anogenital, cutaneous, renal and urologic anomalies, associated with an angioma of lumbosacral localization) e la LUMBAR). In tutti i neonati, anche neurologicamente asintomatici, con EI segmentale, della linea mediana lombosacrale o del perineo, è indicata una RM midollare e addominopelvica.
Nei bambini con emangiomi multipli (definiti arbitrariamente come ≥5 emangiomi generalmente piccoli e localizzati), va esclusa la localizzazione epatica attraverso l’utilizzo dell’ecografia addominale. Raramente, gli emangiomi epatici multifocali possono avere shunt vascolari causa di insufficienza cardiaca. Un'ulteriore complicazione degli emangiomi epatici multipli è l’ipotiroidismo da consumo dovuto all'aumento della produzione dell'enzima inattivante l'ormone tiroideo di tipo 3 iodotironina deiodinasi. Un’altra localizzazione peculiare è quella parotidea, meritevole di trattamento sistemico. L’Emangioma infantile a crescita minima o assente (infantile hemangiomas with minimal or arrested growth, IHMAG): rappresenta una rara varietà di EI. Clinicamente è caratterizzato da chiazze vascolari formate da teleangectasie fini o grossolane con aspetto reticolare su cui successivamente, nel 30% dei casi, compaiono aree di proliferazione rappresentate più spesso da papule angiomatose disposte per lo più alla periferia delle lesioni. Per definizione, la componente proliferativa non deve essere superiore al 30% della superficie totale. L’IHMAG spesso si presenta circondato da un alone di vasocostrizione. Sedi predilette sono la parte inferiore del corpo ed in particolare gli arti, la regione perineale ed i glutei. L’IHMAG si differenzia dall’EI classico non solo per l’aspetto morfologico e la scarsa proliferazione, ma anche per l’epoca di comparsa in quanto è per lo più congenito e per l’assenza, nella maggior parte dei casi, dei fattori di rischio correlati all’EI. Anche l’IHMAG segmentale, specie se localizzato nella parte inferiore del corpo, può associarsi a disrafismo ed anomalie strutturali.
Storia naturale e complicanze
Il ciclo di vita dell’EI è suddiviso in tre fasi:
1) fase rapida proliferativa (0-1 anno); 2) fase di involuzione (1-5 anni); 3) fase involuta (5-10 anni).
1) L’EI raggiunge l’80% del suo volume nella fase iniziale della proliferazione completando quasi sempre l’accrescimento nei primi 5-6 mesi. Solo il 3% degli EI cresce oltre il 9° mese di vita. Le forme superficiali crescono generalmente sino al 5° mese mentre quelle profonde e quelle segmentali si manifestano più tardivamente e continuano a crescere più a lungo (anche sino ai 18 mesi).
2) La fase involutiva è caratterizzata da un rammollimento della lesione e uno scolorimento a partire dall’area centrale con progressiva riduzione del volume e diminuzione della vascolarizzazione della lesione.
3) La fase involuta è caratterizzata da regressione completa o quasi, talvolta con esiti cicatriziali quali cute lassa, atrofia, teleangectasie e/o tessuto fibro-adiposo.
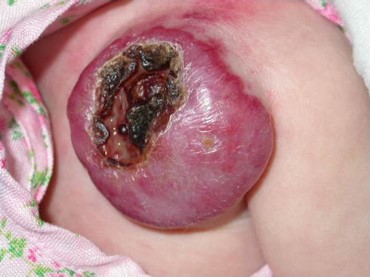
Gli EI superficiali presentano maggior rischio di residui cicatriziali rispetto a quelli profondi. È importante monitorizzare strettamente l’EI quando presenta uno schiarimento nei primi 3 mesi, in quanto può essere predittivo di ulcerazione della lesione piuttosto che di regressione. L'ulcerazione è la complicanza più comune degli emangiomi, particolarmente frequente quando gli emangiomi sono in rapida proliferazione e localizzati in sedi soggette a pressione o traumatismo. L'ulcerazione è sempre dolorosa e può complicarsi con sanguinamento, infezione ed esitare in cicatrici deformanti. Il sanguinamento, sebbene sia una preoccupazione comune tra i genitori, è raramente abbondante e generalmente può essere fermato applicando una pressione diretta. Gli emangiomi delle vie aeree possono presentarsi anche nei bambini che non hanno emangiomi cutanei. Tuttavia, il rischio di emangioma delle vie aeree è maggiore con emangiomi segmentali con distribuzione "a barba", che può includere tutti o alcuni dei seguenti distretti: la cute preauricolare, mandibolare, del labbro inferiore, mento o collo anteriore. La possibilità di emangioma delle vie aeree deve essere considerata in qualsiasi bambino che abbia un emangioma cutaneo a distribuzione cervicofacciale, mandibolare e sviluppi raucedine progressiva o stridore. I neonati affetti hanno maggiori probabilità di manifestare sintomi tra 6-12 settimane, quando la proliferazione dell'emangioma è più rapida. Il coinvolgimento delle vie aeree può essere confermato utilizzando la videolaringoscopia.
Gli emangiomi localizzati in sede periorbitaria, possono compromettere il normale sviluppo visivo, gli emangiomi dell'orecchio possono ostruire il canale uditivo, gli emangiomi della lingua, della cavità orale o del tratto aerodigestivo possono interferire con la suzione, la deglutizione ed il linguaggio, gli emangiomi nucali possono compromettere i normali movimenti di rotazione e flesso estensione del collo.
1.6 Diagnosi
In genere la diagnosi di emangioma infantile è clinica, ma può richiedere l’ausilio dell’Imaging, in particolare dell’eco-color-Doppler, nei casi dubbi o per valutare l’attività proliferativa di una lesione vascolare ai fini del management terapeutico. Il ricorso alla RM/AngioRM diviene mandatorio negli emangiomi segmentali per valutarne l’eventuale estensione, i rapporti con le strutture circostanti o per ricercare anomalie associate come nella PHACES o nella LUMBAR. In alcuni casi, per la diagnosi differenziale con gli altri tumori vascolari, può essere necessario ricorrere all’esame istologico: la positività del GLUT1 è un marker immunoistochimico specifico degli EI, oltre che un fattore predittivo riguardo la risposta al propranololo. Gli emangiomi infantili sono tutti GLUT1 postivi, compresi gli HI-MAG, e quindi tutti potenzialmente sensibili al propranololo.
1.7 Trattamento
Il destino naturale dell’emangioma infantile è l’involuzione, per cui l’approccio terapeutico tradizionale è stato per anni, quello del “wait and see”. Tuttavia, quest’approccio non considerava il rischio consistente, in almeno un terzo dei casi, di inestetismi permanenti, complicanze funzionali o potenzialmente fatali che attualmente possono essere ridotte con trattamenti che arrestano la proliferazione vascolare se avviati precocemente, ovvero nella fase di crescita rapida. Una svolta epocale è stata l’introduzione del propranololo nel trattamento degli EI, in seguito all’osservazione fortuita degli effetti benefici del farmaco, somministrato per il trattamento dell’insufficienza cardiaca in due bambini, che presentavano EI.
Le indicazioni al trattamento comprendono:
1) A rischio per la vita (EI sottoglottici ostruttivi, EI di grosse dimensioni che causano insufficienza cardiaca o epatica)
2) A rischio di impatto funzionale (peri orbitale, nasale, labiale, laringotracheale, articolazioni, canale uditivo)
3) A rischio di esiti estetici con rilevanza psicologica (localizzato sulla glabella, naso, filtro, mento, guancia, labbra con deformità della bocca, ghiandola mammaria nelle femmine) o ulcerati e non responsivi alle medicazioni locali
4) A rischio per anomalie strutturali (es. S. PHACES o LUMBAR)
Strumento utile per valutare l’invio ad un centro specialistico da parte del pediatra curante è l’IHReS, uno score sviluppato dalla Task Force europea per l'emangioma infantile (IHETF), basato su alcuni parametri quali il numero, l’estensione, la localizzazione, il ritmo di crescita dell’emangioma, nonché l’età del paziente.
Il propranololo è un beta-bloccante non selettivo, è l'agente di prima linea per gli emangiomi: nel 2014, la soluzione orale di propranololo cloridrato è stata approvata dalla Food and Drug Administration statunitense per il trattamento dell'emangioma infantile. Il propranololo inibisce la crescita e induce la regressione degli emangiomi infantili. Potenziali meccanismi d'azione del propranololo includono la vasocostrizione, una ridotta espressione del fattore di crescita endoteliale vascolare e del fattore di crescita dei fibroblasti di base e/o l'innesco dell'apoptosi. Il trattamento con propranololo deve essere intrapreso dopo valutazione da parte di dermatologo o altro specialista esperto nella diagnosi e nel trattamento dei tumori vascolari pediatrici e nell'uso del propranololo nei bambini. La valutazione pre-trattamento (in regime di ricovero ordinario o di day hospital) dovrebbe includere: Anamnesi, familiare e personale, con particolare attenzione alle patologie cardiovascolari o respiratorie; esame obiettivo compreso misurazione della frequenza cardiaca, pressione arteriosa e della glicemia; visita cardiologica con elettrocardiogramma nei bambini con: frequenza cardiaca inferiore al range normale per età, storia personale o familiare di anomalie del ritmo e\o della conduzione, storia familiare di cardiopatia congenita o storia materna di malattia del tessuto connettivo; studi di imaging, inclusi l'ecografia cardiaca o la risonanza magnetica cardiaca (MRI), devono essere effettuati nei bambini con emangiomi facciali di grandi dimensioni a rischio di PHACE (≥ 5 cm di diametro) per escludere la possibilità di una grave coartazione aortica, che è una controindicazione all'uso del propranololo.
Nei pazienti affetti da questa sindrome, prima dell'inizio del propranololo è indispensabile praticare anche la RM testa/collo senza e con sequenze angio, a meno che la situazione clinica non richieda un trattamento urgente (p. es., grave ostruzione visiva dovuta a un emangioma orbitale). In tali casi, il propranololo può essere iniziato con una dose più bassa e gradualmente incrementato, fino all’ esito dell'Imaging. Il timing terapeutico è compreso tra le 5 settimane ed i 5 mesi, periodo che coincide con la fase di crescita, nella storia naturale degli emangiomi. In realtà uno studio multicentrico italiano (M. El Hachem et al), ha dimostrato un profilo di sicurezza ed efficacia ottimale, anche nell’utilizzo off label del propranololo, al di fuori del range temporale succitato.
Il trattamento con propranololo è controindicato nei neonati e nei bambini con:
- Shock cardiogeno
- Bradicardia sinusale cronica e significativa documentata
- Ipotensione cronica e significativa documentata
- Blocco cardiaco maggiore di primo grado
- Insufficienza cardiaca
- Storia di broncospasmo o wheezing
- Ipersensibilità al propranololo
- Neonati prematuri con età corretta <5 settimane.
Nella maggior parte dei casi, il trattamento può essere iniziato in un setting di day hospital da un medico con esperienza nella diagnosi e nella gestione degli EI.
L’ospedalizzazione è raccomandata in caso di:
- Neonati ≤ 5 settimane di età;
- Neonati prematuri con età corretta ≥ 5 settimane (età postnatale in settimane meno il numero di settimane pretermine);
- Neonati di qualsiasi età con contesto socioculturale sfavorevole;
- Neonati di qualsiasi età con condizioni di comorbidità che interessano il sistema cardiovascolare o respiratorio, inclusi gli emangiomi sintomatici delle vie aeree;
La dose del farmaco è di 2-3 mg/Kg/die suddivise generalmente in 2 somministrazioni: la dose 3mg/Kg/die viene in genere riservata ai casi gravi (localizzazione laringea, palpebrale) e deve essere preceduta comunque da un periodo di trattamento alla dose di 1 o 2 mg. Per ridurre il rischio di ipoglicemia, il propranololo deve essere somministrato immediatamente, dopo o durante i pasti. Poiché l'effetto del propranololo orale raggiunge i picchi da una a tre ore dopo la somministrazione, si raccomanda che i pazienti vengano monitorati, con la misurazione della frequenza cardiaca e della pressione sanguigna, a una e due ore dopo la dose iniziale e dopo ogni aumento della dose di 0,5 mg/kg/giorno. Ciò è in accordo con le raccomandazioni della Food and Drug Administration statunitense e dell'Agenzia europea del Farmaco. I bambini con emangiomi infantili trattati con propranololo devono essere seguiti a intervalli da uno a tre mesi per la valutazione della risposta e l'aggiustamento della dose relativamente alla crescita ponderale. Il trattamento deve durare almeno 6 mesi o sino al compimento di un anno di età. In caso di recidiva è possibile effettuare un nuovo ciclo di terapia. Sebbene una risposta significativa (riduzione delle dimensioni o risoluzione quasi completa) sia generalmente osservata dopo tre o quattro mesi di trattamento con propranololo, alcuni esperti continuano la terapia fino a quando il bambino raggiunge l'età in cui normalmente inizia la fase di involuzione spontanea. Ciò si verifica in genere intorno a un anno di età, ma può verificarsi prima o dopo a seconda delle dimensioni e del tipo di emangioma. La mancanza di risposta al trattamento con propranololo è rara.
Il rebound, dopo l'interruzione del propranololo è stato osservato in circa il 14-25 % dei bambini. I fattori associati al rischio di recidiva includono la distribuzione segmentale e la profondità dell’emangioma. Alcuni bambini con rebound potrebbero aver bisogno di un secondo ciclo di propranololo. I beta-bloccanti topici (timololo) possono essere usati per trattare le recidive da lievi a moderate. Tuttavia, nella maggior parte dei casi, le recidive lievi non richiedono cure e i genitori possono essere rassicurati sull’involuzione della lesione. Il timololo, presente in commercio come soluzione o gel oftalmico, destinato alla terapia del glaucoma, può essere utilizzato per emangiomi focali sottili e poco estesi come alternativa al “wait and see”. Nei pazienti con emangiomi infantili con controindicazioni al propranololo orale, che non rispondono allo stesso o che manifestano effetti collaterali, è indicato il corticosteroide per via orale. L’impiego di Vincristina è indicato negli EI lifethreatening resistenti al propranololo e al cortisone, o quando questi due farmaci.
La chirurgia è riservata ai casi refrattari alla terapia medica, o proposta come terapia differita degli eventuali esiti al trattamento medico
Conclusioni
Gli EI e le sindromi associate rappresentano sfide diagnostiche e terapeutiche complesse. L’approccio clinico deve essere personalizzato, integrando il ruolo dell’HIRES score per una stratificazione accurata del rischio e la scelta del trattamento ottimale. La collaborazione multidisciplinare è essenziale per gestire le complicanze e migliorare la qualità della vita dei pazienti.
Bibliografia
· Amato B, Ametrano O. Guidelines for Vascular Anomalies by the Italian Society for the study of Vascular Anomalies (SISAV). Int Angiol. 2022 Apr;41(2 Suppl 1):1-130.
· Léauté-Labrèze C, Harper JI, Hoeger PH. Infantile haemangioma. Lancet 2017; 390:85.
· Bruckner AL, Frieden IJ. Hemangiomas of infancy. J Am Acad Dermatol 2003; 48:477.
· Spring S, Noble J, Pope E. Dermacase. Infantile hemangioma. Can Fam Physician. 2009;55(4):379-381.
· Leung AKC, Lam JM, Leong KF, Hon KL. Emangioma infantile: una revisione aggiornata. Curr Pediatr Rev . 2021;17(1):55-69.
· Kilcline C, Frieden IJ. Infantile hemangiomas: how common are they? A systematic review of the medical literature. Pediatr
Dermatol 2008; 25:168.
· Jacobs AH, Walton RG. The incidence of birthmarks in the neonate. Pediatrics 1976; 58:218.
· Alper JC, Holmes LB. The incidence and significance of birthmarks in a cohort of 4,641 newborns. Pediatr Dermatol 1983; 1:58.
· Castrén E, Salminen P, Vikkula M, et al. Inheritance Patterns of Infantile Hemangioma. Pediatrics 2016; 138.
· Chiller KG, Passaro D, Frieden IJ. Hemangiomas of infancy: clinical characteristics, morphologic subtypes, and their relationship to race, ethnicity, and sex. Arch Dermatol 2002; 138:1567.
· Drolet BA, Esterly NB, Frieden IJ. Hemangiomas in children. N Engl J Med 1999; 341:173.
· Enjolras O, Gelbert F. Superficial hemangiomas: associations and management. Pediatr Dermatol 1997; 14:173.
Dott.ssa Filomena Barbato
Dott. Antonio Prisco
Dott.ssa Orsola Ametrano